🧠 ใครบ้างมีความเสี่ยง MCI และหากประเมินเบื้องต้นแล้วพบว่าเสี่ยง…ควรทำอย่างไรต่อ?
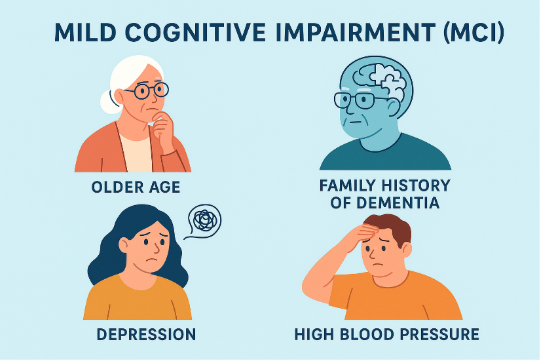
ภาวะการรู้คิดเสื่อมเล็กน้อย (Mild Cognitive Impairment: MCI) คือระยะกึ่งกลางระหว่าง “สมองปกติ” กับ “ภาวะสมองเสื่อม (Dementia)” ผู้มี MCI มักเริ่มมีอาการหลงลืม การคิดหรือวางแผนช้าลง แต่ยังใช้ชีวิตประจำวันได้เอง การตรวจพบตั้งแต่เนิ่น ๆ ช่วยให้มีโอกาสฟื้นฟูสมอง และป้องกันการเข้าสู่ภาวะสมองเสื่อมได้มากขึ้น1
Q1 : ใครบ้างที่มีความเสี่ยงต่อ MCI?
- อายุ ≥ 50 ปีขึ้นไป
ผู้สูงอายุเป็นกลุ่มเสี่ยงหลัก งานวิจัยในชุมชนประเทศจีนพบว่า ในผู้ที่อายุ ≥ 50 ปี มีถึง 26.7% พัฒนาเป็น MCI ภายใน 2 ปี 2
- ระดับการศึกษาต่ำ
ผู้ที่จบเพียงระดับประถม หรือต่ำกว่า เสี่ยงเป็น MCI มากกว่าผู้มีการศึกษาสูงถึง 2.8 เท่า (RR=2.79) เพราะมี “cognitive reserve” ต่ำกว่า2,3
- ประวัติโรคหลอดเลือดสมอง
- โรคหลอดเลือดสมองตีบ (cerebral infarction) เพิ่มความเสี่ยง 1.5 เท่า
- โรคเลือดออกในสมอง (cerebral hemorrhage) เพิ่มความเสี่ยง 3.2 เท่า2
- โรคประจำตัวเรื้อรัง
เช่น เบาหวาน ความดัน ไขมันในเลือดสูง โรคหัวใจ ซึ่งส่งผลต่อหลอดเลือดสมองโดยตรง4
- พฤติกรรม และวิถีชีวิต
การนอนน้อย เครียดเรื้อรัง สูบบุหรี่ ดื่มแอลกอฮอล์มากเกินไป ล้วนเพิ่มความเสี่ยง ในทางกลับกัน การดื่มชาเป็นประจำ ช่วยลดความเสี่ยง MCI ลงได้ประมาณ 31% จากฤทธิ์ต้านอนุมูลอิสระของชา5
- ภาวะซึมเศร้า และขาดการเข้าสังคม
สมองที่ไม่ได้รับการกระตุ้นด้านอารมณ์ และสังคมจะเสื่อมเร็วกว่าปกติ6
Q2 : หากประเมินเบื้องต้นแล้วพบว่า “เสี่ยง MCI” ควรทำอย่างไรต่อ?
ขั้นตอนที่ 1️⃣: พบแพทย์เฉพาะทาง
แพทย์เฉพาะทางด้านสมอง อายุรแพทย์ผู้สูงอายุ หรือจิตแพทย์ผู้สูงอายุ จะประเมินซ้ำ เพื่อยืนยันผล และแยกจากโรคอื่น เช่น ภาวะซึมเศร้า การขาดวิตามิน B12 หรือผลข้างเคียงจากยา
ขั้นตอนที่ 2️⃣: การตรวจด้วย “แบบทดสอบทางจิตวิทยา”
เป็นการประเมินความสามารถของสมองในหลายด้าน เช่น ความจำ ความสนใจ ภาษา การวางแผน และการตัดสินใจ
แพทย์อาจเลือกใช้เครื่องมือที่เหมาะสมกับอายุและระดับการศึกษา เช่น
- MoCA (Montreal Cognitive Assessment)
- MMSE (Mini-Mental State Examination)
- Clock Drawing Test หรือ Trail Making Test
- แบบทดสอบเฉพาะด้าน (เช่น verbal fluency, digit span, story recall)
ผลทดสอบเหล่านี้จะช่วยแยกได้ว่าอาการ “ลืม” นั้นอยู่ในระดับปกติของวัย หรือเริ่มเข้าสู่ภาวะ MCI7
ขั้นตอนที่ 3️⃣: ตรวจสุขภาพร่างกายและสมอง
เพื่อค้นหาสาเหตุที่อาจแก้ไขได้ และประเมินความผิดปกติของสมองโดยตรง แพทย์อาจส่งตรวจ
การตรวจเลือดทั่วไป
- น้ำตาล ไขมัน วิตามิน B12 ไทรอยด์
การตรวจสมอง (Neuroimaging & Biomarker Assessment)
- MRI: ดูการหดตัวของสมอง โดยเฉพาะบริเวณ hippocampus8
- PET Scan (FDG-PET หรือ Amyloid PET): ตรวจการใช้พลังงานสมองหรือการสะสมของโปรตีน amyloid/tau
- CSF Biomarkers: ตรวจระดับ Aβ42, total tau, p-tau เพื่อแยก MCI due to Alzheimer’s pathology9
- Blood-based Biomarkers (BBM): เช่น plasma Aβ42/40 ratio, p-tau217, NfL — สะดวกและไม่รุกราน10
🔄 หมายเหตุ:
- หากผลตรวจ ปกติ แต่ยังอยู่ในกลุ่มเสี่ยง → ควรเข้าสู่ “ขั้นตอนที่ 4” เพื่อเริ่มปรับพฤติกรรมเสริมสมอง
- หากผลตรวจ พบความผิดปกติของโปรตีน β-amyloid หรือ tau → แพทย์อาจพิจารณาเริ่มการรักษาด้วย ยากลุ่ม monoclonal antibody ซึ่งออกฤทธิ์กำจัดโปรตีน amyloid ในสมอง ทั้งนี้ขึ้นอยู่กับ สภาพร่างกาย โรคร่วม และความพร้อมของผู้ป่วย รวมถึงการติดตามผลข้างเคียงอย่างใกล้ชิด11,12
ขั้นตอนที่ 4️⃣: ปรับพฤติกรรมเสริมสมอง
- อาหารสมดุล: แบบ Mediterranean หรือ DASH diet
- ออกกำลังกาย: อย่างน้อย 150 นาทีต่อสัปดาห์
- นอนหลับให้เพียงพอ: 7–8 ชั่วโมง/คืน
- ฝึกสมอง: เกมความจำ อ่านหนังสือ เรียนรู้สิ่งใหม่
- เข้าสังคม: พบปะเพื่อนหรือทำกิจกรรมกลุ่ม
ขั้นตอนที่ 5️⃣: ติดตามประเมินซ้ำทุก 6–12 เดือน
เพื่อตรวจการเปลี่ยนแปลงของสมรรถภาพสมองและวางแผนการดูแลอย่างต่อเนื่อง
🔹 สรุป
การวินิจฉัย และดูแลภาวะ MCI จำเป็นต้องใช้ทั้ง “การประเมินทางจิตวิทยา” และ “การตรวจทางสมอง” ร่วมกัน เพื่อระบุความเสี่ยง และแนวทางดูแลที่เหมาะสม การเริ่มต้นตั้งแต่ช่วง “ยังจำได้แต่เริ่มลืม” คือกุญแจสำคัญในการชะลอภาวะสมองเสื่อ และรักษาคุณภาพชีวิตในระยะยาว
🔹 เอกสารอ้างอิง (Vancouver Style)
- Petersen RC, Lopez O, Armstrong MJ, et al. Neurology. 2018;90(3):126–35.
- Zhang NJ, Qian ZD, Zeng YB, et al. Eur Rev Med Pharmacol Sci. 2022;26:8852–8859.
- Meng X, D’Arcy C. PLoS One. 2012;7:e38268.
- Livingston G, Huntley J, Sommerlad A, et al. Lancet. 2020;396:413–46.
- Liu X, Du X, Han G, Gao W. Oncotarget. 2017;8:43306–43321.
- Geda YE, Roberts RO, Knopman DS, et al. Arch Neurol. 2006;63(3):435–40.
- Nasreddine ZS, Phillips NA, Bédirian V, et al. The Montreal Cognitive Assessment, MoCA: a brief screening tool for mild cognitive impairment. J Am Geriatr Soc. 2005;53:695–699.
- Jack CR Jr, Petersen RC, Xu YC, et al. Neurology. 1999;52(7):1397–1403.
- Hansson O, Blennow K, Zetterberg H. Nat Rev Neurol. 2023;19(1):51–64.
- Palmqvist S, et al. Nat Med. 2020;26:387–97.
- van Dyck CH, et al. N Engl J Med. 2023;388:9–21.
- Mintun MA, et al. N Engl J Med. 2021;384:1691–1704.